Saúde
Medicação contra o câncer de mama mais agressivo é desenvolvida no Brasil
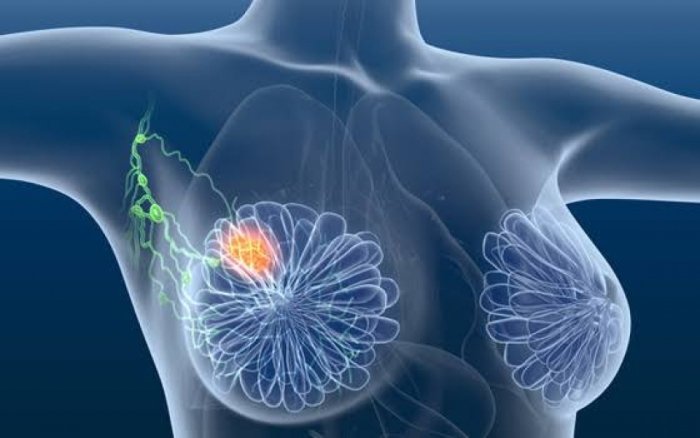
Mais de 66 mil novos casos de câncer de mama foram diagnosticados durante o ano passado no Brasil, de acordo com estimativa do Instituto Nacional do Câncer (INCA). Em 2019, mais 18,2 mil pessoas faleceram em decorrência da doença, sendo 18.068 mulheres e 227 homens, segundo o Atlas de Mortalidade por Câncer (SIM). Diante desses números, o tumor já é a primeira causa de morte por câncer na população feminina brasileira, com 14,23 óbitos a cada 100 mil mulheres. Inclusive, já supera o câncer de pulmão.
Nesse cenário, pesquisadores brasileiros trabalham em alternativas e no desenvolvimento de novas terapias para o tratamento de diferentes tipos de câncer de mama. Este é o caso da startup PHP Biotech que, em estudos pré-clínicos, avalia a eficácia de um tratamento nanomolecular contra um tipo específico da doença, o Triplo-Negativo. Atualmente, não há, no mercado, uma alternativa de terapia específica para esse tumor. Nessa empreitada contra o câncer de mama, a healthtech tem como parceiros a Kaivo Biotech e a FCJ Venture Builder.
Para aperfeiçoar o tratamento deste tipo de câncer, a equipe investigou moléculas da biodiversidade brasileira e construiu uma alternativa sintética, que poderá ser usada em larga escala. Inclusive, o primeiro lote da molécula 3-NAntc já foi produzido nos Estados Unidos e estão sendo usadas nos testes contra o triplo-negativo em laboratório. In vitro, equipe já observou que, quando aplicada em células tumorais, mais de 30% morreram, com uma única aplicação.
Para entender como a molécula da biodiversidade brasileira pode contribuir no combate ao câncer de mama Triplo-Negativo, o Canaltech conversou com Patrícia Alves, doutora pela Faculdade de Farmácia da Universidade do Porto (FFUP) e biotecnóloga responsável pela pesquisa.
Quais são os principais tipos de câncer de mama?
“Hoje, são 4 tipos de câncer de mama principais e são definidos, justamente, pelos receptores [proteínas que podem se conectar a determinados componentes do sangue] que eles apresentam na membrana plasmática”, explica Alves, da PHP Biotech. O tipo Luminal “expressa receptores hormonais, tanto de estrogênio quanto de progesterona” e se divide em A e B, através de um fator de proliferação, que é o Ki-67.
O terceiro tipo é o Her-2 Enriquecido, reconhecido por apresentar uma grande quantidade do receptor Her-2 de proliferação. Por fim, há o Triplo-Negativo que “não tem receptor de estrogênio, de progesterona e o Her-2”, explica a pesquisadora. Para compreender visualmente a diferença entre esses tipos, vale conferir a imagem a seguir:
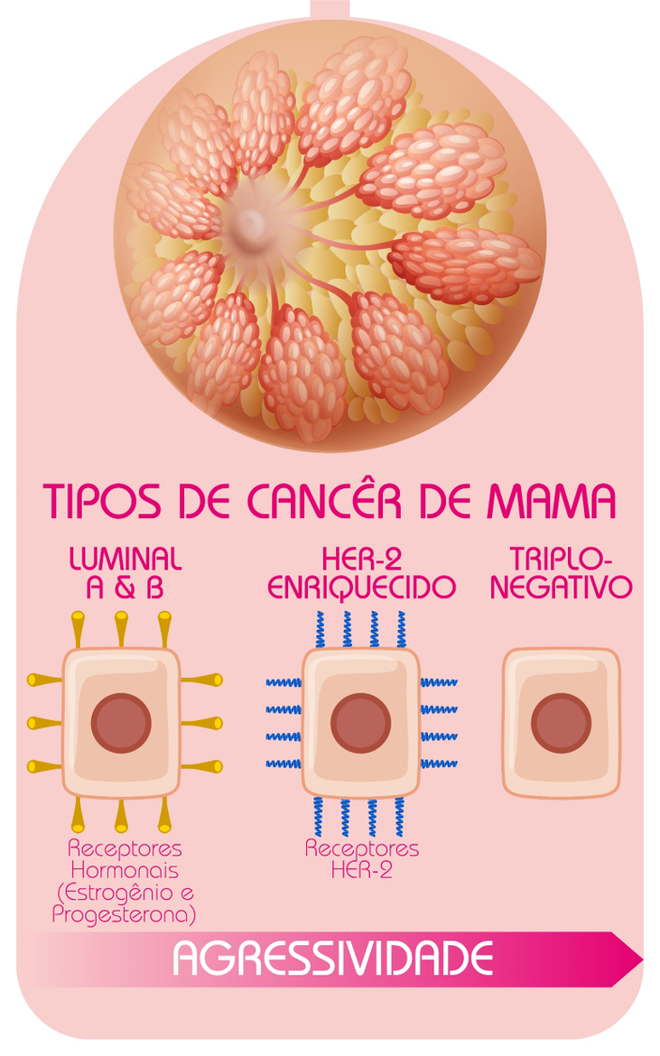
Segundo o Instituto Oncoguia, o câncer Triplo-Negativo é um subtipo agressivo e que pode levar a óbito entre 30% e 40% das mulheres que o desenvolvem, já que não há um tratamento específico. “As terapias que existem disponíveis para outros tipos de tumor não ajudam [de forma substancial] o tratamento do Triplo-Negativo, justamente porque não têm algo conhecido [como um receptor]. Como ele não tem um elemento conhecido, se utiliza a terapia citotóxica, uma terapia mais geral”, explica Alves.
Em outras palavras, os quimioterápicos que são utilizados para este tipo de câncer são aproveitados de outras terapias contra tumores. Nesses casos, o foco do medicamento está em impedir a proliferação do tumor e, não, em algo específico, que diferencie o tumor da célula benigna. Caso um tratamento afete tanto as células tumorais quanto as benignas, é possível que o paciente não melhore ou ainda apresente uma piora no quadro.
“Essa molécula [3-NAntc] funciona [em testes] tanto para o câncer Triplo-Negativo quanto para o Luminal A”, comenta Alves. No entanto, foi definido como estratégia para o desenvolvimento do medicamento focar no tipo que não conta com uma terapia específica. Em um segundo momento, a pesquisa também deve se voltar para o segundo tipo.
Pesquisas com a molécula da biodiversidade brasileira
Um dos pontos interessantes da molécula é que ela foi descoberta a partir da biodiversidade brasileira. Isso significa que ela estava presente em elementos da natureza do país, como extratos da flora, da fauna ou do reino Fungi. No momento, a equipe ainda não pode compartilhar qual é a exata origem dessa molécula por questões estratégicas. Independente dessa origem, o procedimento de desenvolvimento é o mesmo. Primeiro a equipe observa para ver qual é a potencial ação do extrato: por exemplo, antitumoral ou antimicrobiana.
Em segundo lugar, esse extrato é dividido em diferentes porções e esse procedimento é feito por cromatografia Líquida (HPLC), onde se verifica se a parte preserva com a função principal. Essa passo é fundamental porque um extrato pode ter de 1,4 a 1,6 mil moléculas diferentes e nem todas são necessariamente benéficas para aquela finalidade. Em seguida, ocorre um trabalho com espectrometria de massa para detectar cada molécula que está ali dentro daquela seleção.

“Já sabíamos que existia essa molécula [mãe] na biodiversidade brasileira e que era um antitumoral muito potente, mas, em simultâneo, era muito tóxica para as pessoas”, explica a pesquisadora. Por isso, foi tão importante a análise desse extrato em inúmeros pedaços, em um processo de pesquisa que já completa 15 anos.
“Hoje, temos uma molécula que é sintética, com escalabilidade industrial. Notamos que ela continua — até um pouco mais promissora — com a atividade antitumoral”, explica a pesquisadora. Essa melhora na atividade se deu porque na formulação nanomolecular, em laboratório, foi possível “retirar grande parte da citotoxicidade [da molécula] para as células benignas que estavam na molécula mãe”, o que foi possível alcançar após vários testes com protótipos da molécula sintética.
O que falta para a aprovação do novo tratamento?
Atualmente, a equipe de pesquisa sabe que “essa molécula [sintética] afeta seis vezes mais uma célula tumoral do que uma célula benigna. Isso, em comparação com o que já temos no mercado, nos chamou a atenção”, explica Alves. Através da quimioterapia para o Triplo-Negativo, o tratamento geralmente adotado foca tanto nas células tumorais quanto nas benignas. “Quando você vê a proporção da quimioterapia disponível no mercado, pelo menos in vitro, é 2 para 1. Você mata 2 células tumorais enquanto mata uma benigna”, explica a cientista, detalhando a importância da descoberta.
Agora, a próxima etapa do projeto é a conclusão dos testes pré-clínicos. No processo de desenvolvimento, ainda estão abertas algumas questões como a via de aplicação, o que poderá ser feito através de comprimidos ou de uma injeção intravenosa, e os estudos ainda não foram divulgados em revistas científicas. Em um segundo momento, também deve ser solicitada a autorização dos testes da molécula em humanos através de uma agência regulamentadora, como a Food and Drug Administration (FDA), nos Estados Unidos, ou a Agência Nacional de Vigilância Sanitária (Anvisa).
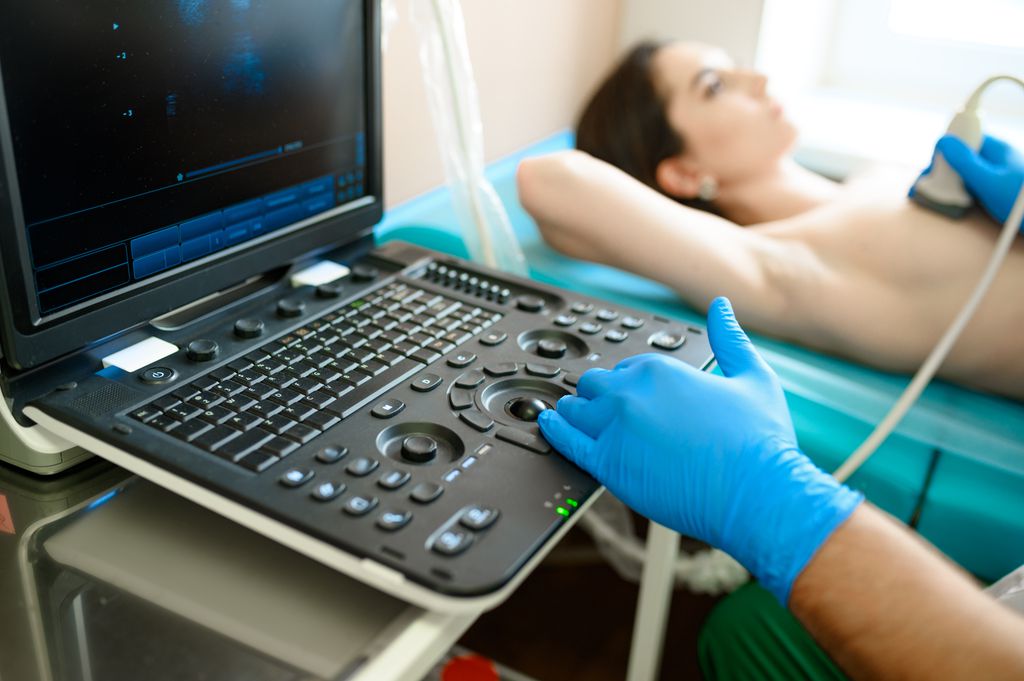
Vale lembrar que, mesmo com o desenvolvimento de novas técnicas para o tratamento de pacientes com câncer de mama, a mamografia é o principal exame preventivo para identificação de tumores e o diagnóstico precoce pode salvar vidas, ainda mais em mulheres acima dos 40 anos.